| 基本信息 | 更多 | 【中文】
氢硫酸 | 【英文名称】
H2S
HYDROGEN SULFIDE
HYDROGEN SULFIDE, SOLID
HYDROGEN SULFIDE WATER
HYDROGEN SULFIDE WATER, SAT
HYDROGEN SULPHIDE
Acide sulfhydrique
acidesulfhydrique
acidesulfhydrique(french)
acidesulphhydrique
Dihydrogen monosulfide
Dihydrogen sulfide
dihydrogenmonosulfide
dihydrogensulfide
Hepatic acid
Hepatic gas
Hydrogen monosulfide
Hydrogen sulfide (H2S)
Hydrogene sulfure
hydrogenesulfure | 【CAS】
7783-06-4 | 【中文名称】
硫化氢
硫化氢(>99.5%)
氢硫酸
硫化氢(液体)
硫氢化合物
液体硫化氢 | 【EINECS 编号】
231-977-3 | 【分子式】
H2S | 【MDL 编号】
MFCD00011444 | 【分子量】
34.08 | 【MOL 文件】
7783-06-4.mol | 【所属类别】
无机化工产品: 无机盐: Co硫化物及硫酸盐 |
| 物理化学性质 | 回目录 | 【外观性质】
无色、有恶臭的气体。 | 【溶解性】
溶于水、乙醇。 | 【熔点 】
−85 °C(lit.)
| 【沸点 】
−60 °C(lit.)
| 【蒸气密度】
1.19 (15 °C, vs air)
| 【蒸气压】
252 psi ( 21 °C)
| 【Merck 】
13,4823 |
| 应用领域 | 回目录 | 【用途一】
可用于转化硫黄和硫酸,生产硫化钠和硫氢化钠,或用于生产有机硫化合物如噻吩、硫醇和硫醚等 | 【用途二】
用于分离和鉴定金属离子、精制盐酸和硫酸、制元素硫 | 【用途三】
用于合成荧光粉,电放光、光导体、光电曝光计等的制造。有机合成还原剂。用于金属精制、农药、医药、催化剂再生。通用试剂。制取各种硫化物。 | 【参考质量标准】
参考标准| 指标名称 | 指标 | | 含量(H2S,液相)/%≥ | 99.0 | | 氮(N2)/%< | 0.007 | | 氧(O2) | %<0.003 | | 水分(H2O)/%< | 0.003 | | 烯烃(CnHm)/%< | 0.1 | | 外观 | 无色、有恶臭、有毒的酸性气体 |
|
| 制备方法 | 回目录 | 【方法一】
将20%~30%磷酸慢慢地从分液漏斗滴到Na2S?9RO浓水溶液中,将所产生的气体经无水氯化钙与五氧化二磷干燥,制得硫化氢气体,经液化压入钢瓶。
用硫黄和氢直接合成制得硫化氢纯度高。 |
| 7783-06-4(安全特性,毒性,储运) | 回目录 | 【爆炸物危险特性】
与空气混合易爆 | 【储运特性】
库房通风低温干燥; 与硝酸、强氧化剂分开存放 | 【毒性分级】
中毒 | 【急性毒性】
吸入-大鼠LC50:666毫克/立方米;吸入-小鼠LC50:951毫克/立方米/1小时 | 【可燃性危险特性】
易燃; 燃烧产生有毒氮氧化物烟雾 | 【类别】
有害气体 | 【灭火剂】
雾状水、砂土、泡沫 | 【职业标准】
TWA 15 毫克/立方米; STEL 23 毫克/立方米 |
| 常见问题列表 | 回目录 | 【硫化氢】
氢硫酸是硫化氢的水溶液,硫化氢是硫的氢化物,化学式为H2S。一种无色、有恶臭味(臭鸡蛋味)的剧毒气体。能溶于水和乙醇,比重为1.1906。熔点-85.5°C,沸点-60.4°C,临界温度100.4°C,临界压力90.06×105帕。自燃点为260°C,具有可燃性,遇火星能引起爆炸燃烧,与空气相混时,能引发爆炸,爆炸极限为4%~44%(体积)。能与多种离子起化学作用,生成不溶于水的硫化物,能使铜、银表面变黑。广泛存在于金属冶炼、天然气 、盐酸和硫酸等的制造工业中。在制造硫酸盐纸浆、人造丝、人造棉、橡胶、二硫化碳等各种硫化物时,常有硫化氢气体排出。在一些化学反应中,含硫化合物不稳定也会分解出硫化氢,如:炼焦、精制石油及金属冶炼中,硫化氢作为一种常规废气,极易泄漏到空气中。硫化染料分解也可放出硫化氢气体。
硫化氢在水中电离,是个二元弱酸, 称为氢硫酸:
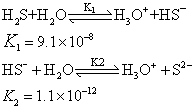
图1:硫化氢在水中电离生产氢硫酸
在空气中, 氢硫酸能被氧逐渐氧化, 析出硫磺而变混浊故必须在使用前临时配制。硫化氢化学性质不稳定,加热时会分解为氢和硫。在空气中燃烧, 生成水和二氧化硫。在不足的空气中燃烧, 可得到单质硫。硫化氢中的硫易于给出电子, 所以它是一种很好的还原剂。如在酸性介质中, 它能将Fe3+还原成Fe2+, 将Br2还原成Br-, 将MnO-4还原为Mn2+,将Cr2O2-7还原成Cr3+,将HNO3还原成NO2等,而硫化氢则被氧化成单质硫或亚硫酸盐或硫酸盐。在潮湿的空气中硫化氢和SO2反应生成单质硫 (歧化反应的逆反应)。硫化氢能使银、铜等制品表面变黑, 与许多金属离子作用, 生成不溶于水或酸的硫化物沉淀。在实验室中常用于分离、鉴定金属离子。硫化氢在实验室中常用FeS与稀盐酸作用来制取。氢与硫只在加热时才反应生成硫化氢。
| 【水中溶解度(g/100ml)】
每100毫升水中的溶解克数:
0.33g/20℃ | 【毒性】
有毒!主要经呼吸道吸收而引起全身中毒,是一种化学性窒息性气体。接触浓度超过700×10-6时产生急性中毒。如不及时救治,就会死亡。低浓度气体能刺激呼吸器官和眼睛,还有头痛、眩晕、虚弱等症状。出现咳嗽、结膜炎。操作时必须穿戴包括氧气防毒面具的全身防护服。对吸入蒸气的患者脱离污染区,安置在空气新鲜的地方并保暖。严重者须就医诊治。如果呼吸停止,须立即进行人工呼吸。眼睛受刺激须用大量水冲洗,并就医诊治。 |
|
|